영상강의 ▲
Alkyne의 명명법과 성질
<Alkyne의 명명법>
1. 모체는 3중결합이 있는 것 中 가장 긴 것이어야 한다.
3중 없는 것 중 더 긴게 있더라도.. 걘 모체가 될 수 없음
-yne으로 끝내고, 3중결합의 번호를 함께 써준다
ex. 2-heptyne 혹은 hept-2-yne
사진 속 예제는 예를 들어서
1. 3중 결합 있는 것 중 가장 긴 건 6개 >> hexyne
2. 첫 작용기 숫자 최소가 되도록 번호 매김 >>hex-3-yne
3. 작용기들 이름 매기고, 알파벳 순으로 나열 >> 2-methylhex-3-yne

<Alkyne은 base, nucleophile, acid>

alkyne의 3중결합은 sp 오비탈의 시그마 결합 하나, p 오비탈의 파이 결합 2개 >> 3중결합
* 전자가 3중결합에 많아서 base나 nucleophile로 작용 가능 >> 치환 반응
* C에 달린 H가 sp 오비탈에 존재함. sp 오비탈은 s오비탈로서의 성격이 커서 안정하고, 전자를 잘 가지고 있음.
따라서 양성자가 떨어져나갔을 때, 짝염기 상태가 (alkane, alkene에 비해) 비교적 안정함.
즉 terminal 부분은 acid로 작용할 수 있음.

단 acid로 작용하려면 충분히 강한 base가 필요함.
alkyne의 짝염기 상태보다 불안정한 base를 넣어주어야 함
ex. NH2-, H-, C2H5-
Alkyne의 합성, alkylation

<Alkyne의 합성>
dihalide를 다음과 반응시킴
1) 2 NaNH2 (충분히 강한 염기) / NH3
2) H2O
*dihalide는 하나의 C에 2개 모두 붙은 geminal, 나란한 C에 각각 하나 붙은 vicinal 모두 가능함.
베타 탄소의 H로서의 H가 2개 있어야 함
이 둘에 대해 E2 반응이 2번 일어난다고 생각하면 된다.
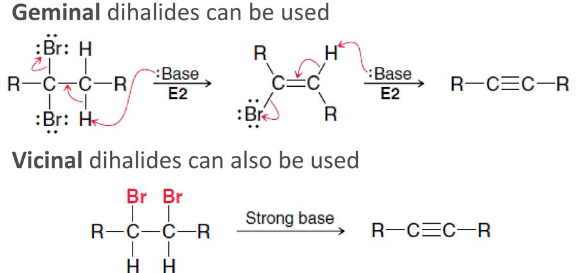
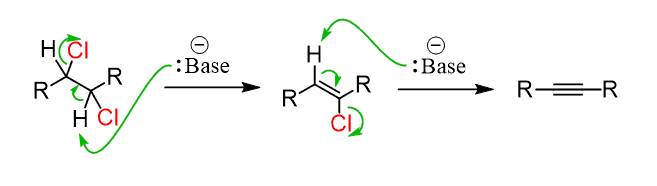
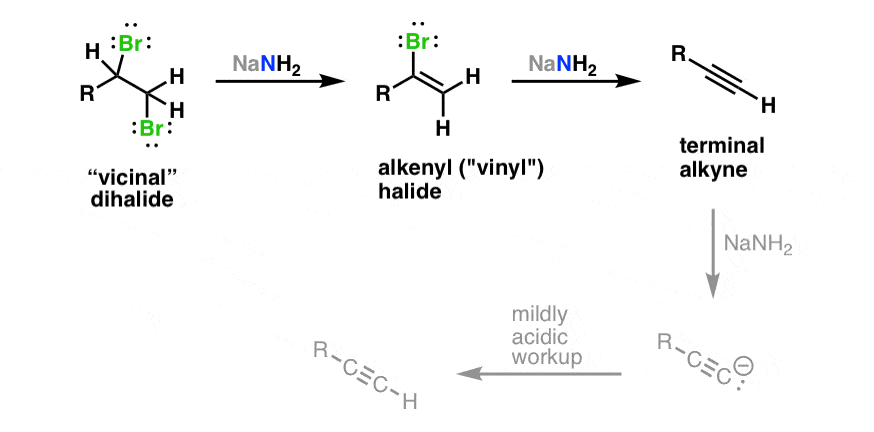
두 번째에서, alkene을 또 E2반응하기 위해서 충분히 센 염기(NH2- 등)가 필요하다
다만 센 염기라 완성물인 alkyne을 산으로 삼아, terminal 양성자를 떼어내버릴 수도 있음
그래서 terminal R기가 H인 경우에는, 더 강산인 H2O를 나중에 반응시켜서 H를 붙여줌
<terminal alkyne의 alkylation>
alkyne을 다음과 반응
1) NaNH2 / NH3 (1당량만)
2) RX
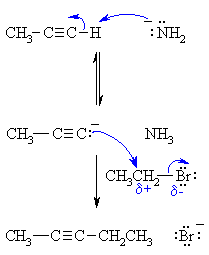
붙이고 싶은 alkyl기를 할로젠(X)와 결합한 RX와 반응시킴
그러면 SN2처럼 반응해서 R기가 붙게 된다
이때 alkyl기는 1차여야 한다
왜냐면 2차 이상부터는 E2가 더 우세해지기 때문이다
Alkyne의 첨가반응
| H, X | H OH & tautomerization | H H | X X |
| Markovnikov -1당량이면 alkene -2당량(xs)면 alkane HX |
Markovnikov 산의 tautomerization 1) Hg(OAC)2, H2O 2) NaBH4 |
cis를 거쳐 alkane까지 H2, Pt |
X2 -1당량이면 trans alkene -2당량(xs)면 alkane |
| anti-Markovnikov HBr ROOR *E/Z 형태 주의 |
anti-Markovnikov 염기의 tautomerization 1) BH3 THF 2)H2O2 NaOH |
cis alkene H2, Pt |
|
| trans alkene H2, Pt |
<1> H X (hydrohalogenation)
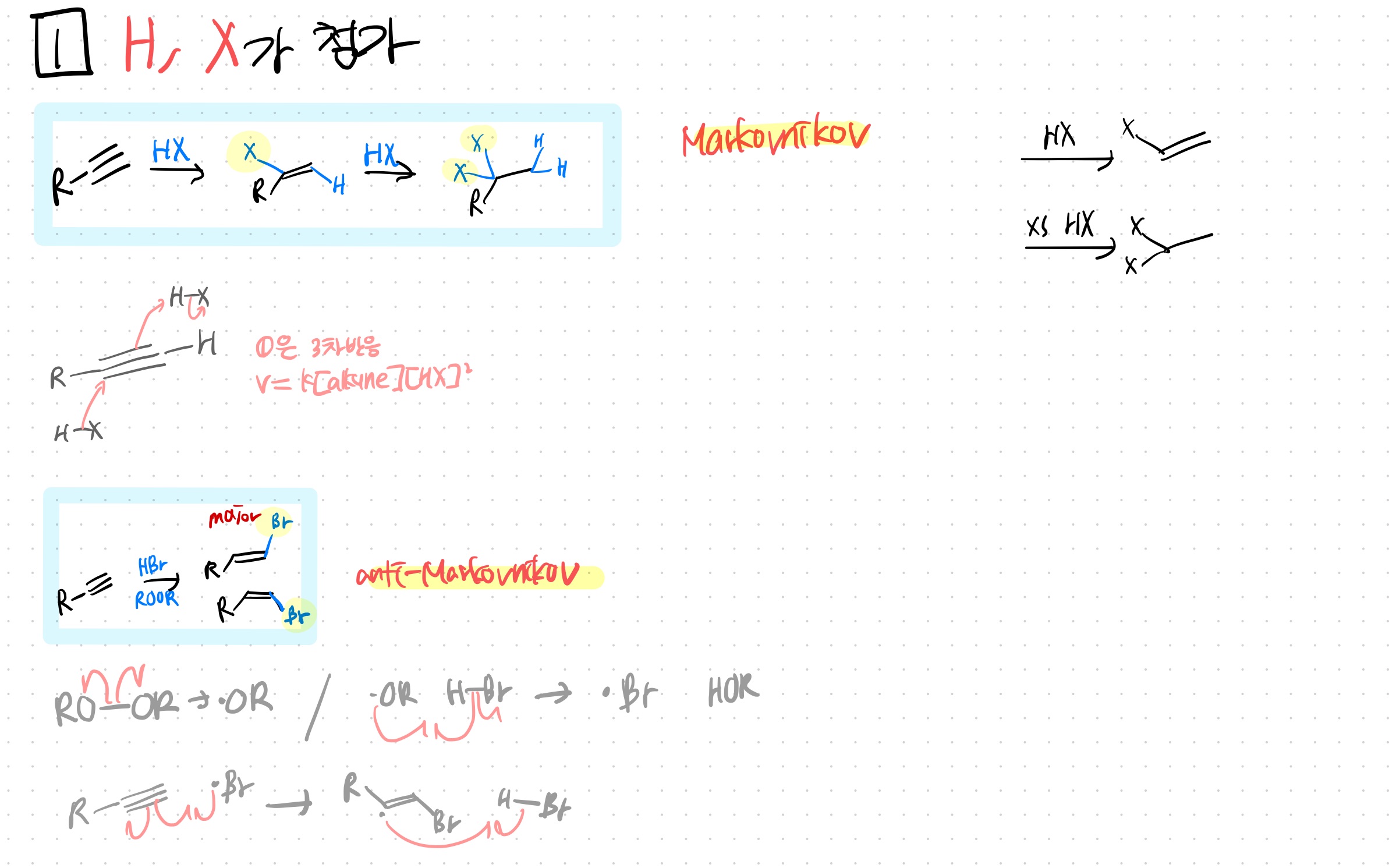
(1) HX와 반응
-Markovnikov : 치환기 많은 쪽에 X, 적은 쪽에 H
-1당량이면 alkene
-2당량(혹은 xs)이면 alkane
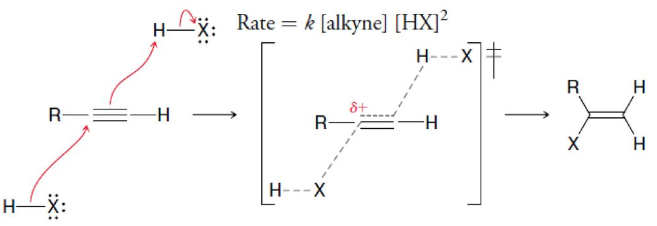
alkene 때와 유사하게, 양전하가 차수가 높은 곳에 위치하는게 좋기 때문에 Markovnikov임
단, 3차 반응인데, H와 X 붙는게 거의 동시에 이루어지기 때문이다
HBr, ROOR과 반응
-anti Markovnikov : 치환기 많은 쪽에 H, 적은 쪽에 X (radical을 거치기 때문)
-1당량이면 alkene
-2당량(혹은 xs)이면 alkane
E/Z 둘 다 나옴 주의, major 있음
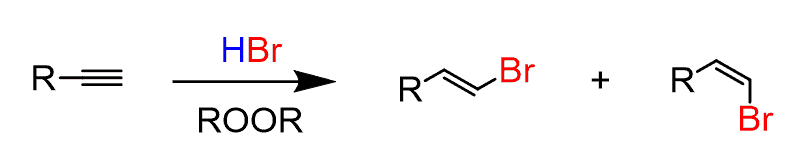
alkene이 될 때 E/Z 둘 다 나옴 주의
더 안정한 건 steric한 애들끼리 엇갈린 애다. 걔가 major임
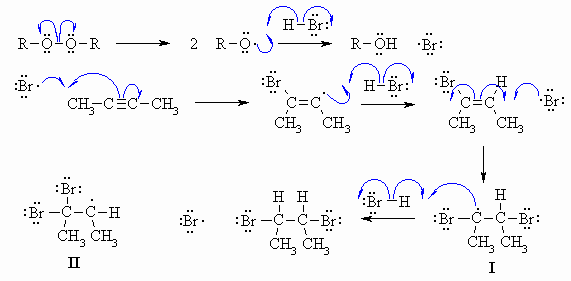
alkene 때와 마찬가지로 anti Markovnikov함
라디칼을 거치기 때문임
alkene 상태에서 한 번 더 반응하면 alkane이 됨
<2> H OH (hydration) & tautomerization
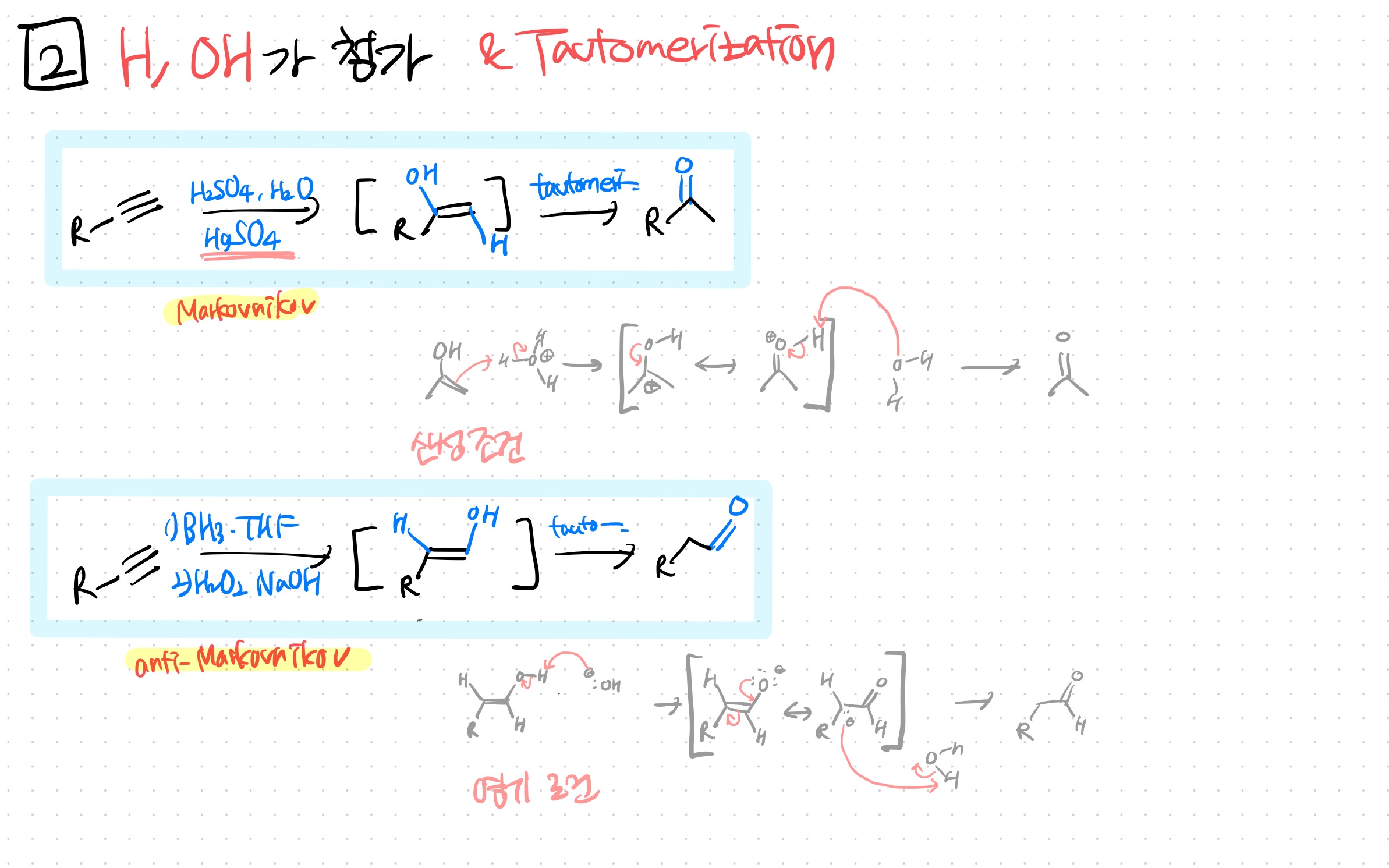
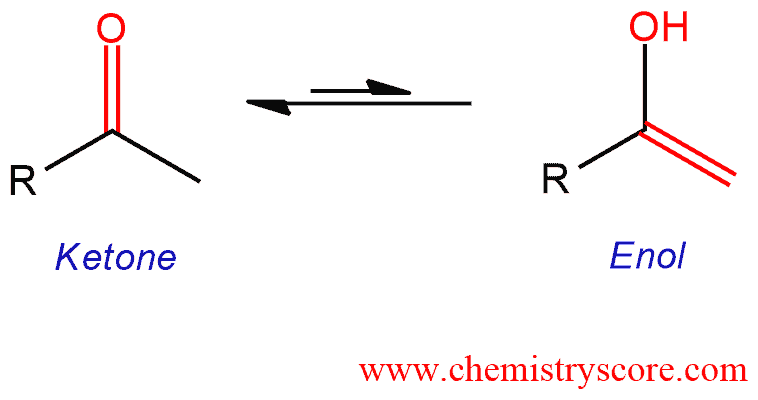
두 가지 반응이 있는데 둘 다 토토머화를 거친다.
enol이 생기면 재빠르게 더 안정한 keto로 바뀌는 게 토토머화하다.
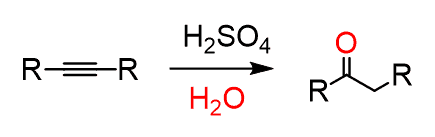
(1) 1) Hg(OAc)2 H2O
2) NaBH4
(oxymercuration demercuration)
-Markovnikov : 치환기 많은 쪽에 OH, 적은 쪽에 H
-이후 산에서의 tautomerization을 거쳐 keto가 됨
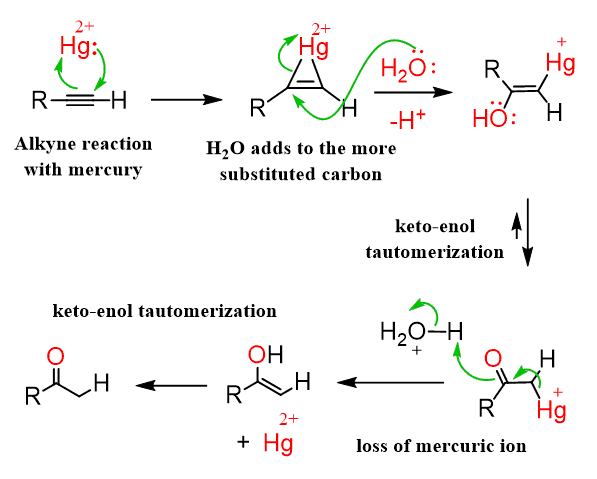
alkene때와 유사하다. Hg가 양쪽에 붙어서 부분 양전하가 생기게 되는데,
부분 양전하라도 차수가 높은 쪽에 위치하는 게 안정해서 Markovnikov를 따른다.
그래서 차수가 많은 쪽에 OH가 붙고...
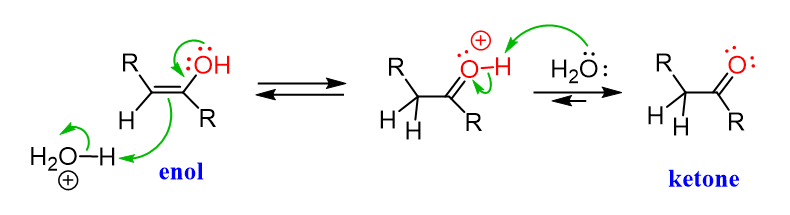
이후 acid catalyzed tatutomerization을 해서 enol이 ketone으로 바뀐다.
ketone이 훨씬 안정해서 ketone으로 빠르게 바뀌기 때문에 반응물은 꼭 ketone으로 써줘야 한다!
산성 조건에서의 tautomerization을 거친다
산의 양성자를 빼앗은 뒤 공명을 거치고, 새로운 양의 형식전하 차리가 생기면 약염기가 공격한다 (SN1 후반부 과정처럼)
(2) 1) BH3 THF
2) H2O2 NaOH
(hydroboration oxidation)
-Markovnikov : 치환기 적은 쪽에 OH, 많은 쪽에 H
-이후 염기에서의 tautomerization을 거쳐 keto가 됨
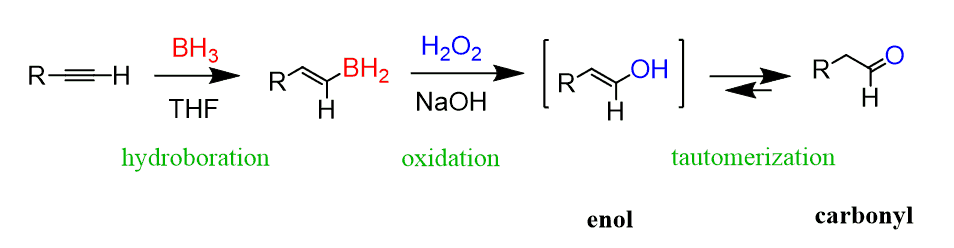
적은 쪽에 OH가 붙고, 바로 tautomerization을 거쳐 aldehyde가 된다
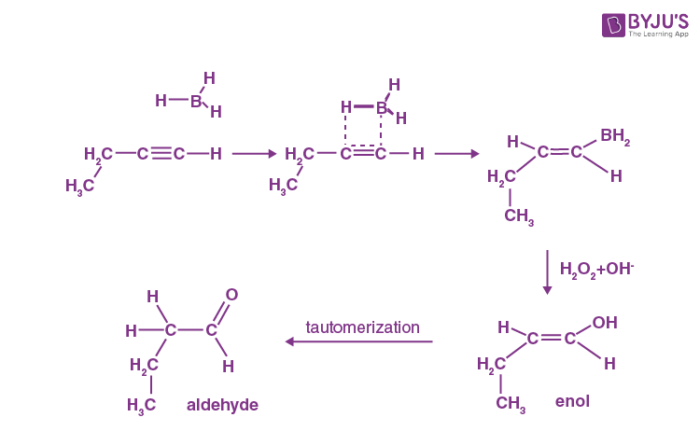
alkene 때와 유사하다.
BH2와 H가 동시에 붙는데, BH2는 덜 steric한 자리에 접근하기 쉬우니 anti-Markovnikov를 따른다
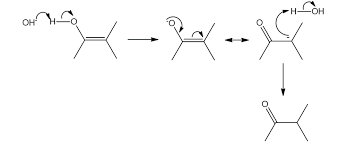
이후 바로 염기성 조건에서의 tautomerization을 거친다
염기에 의해 OH가 양성자 하나를 빼앗긴 뒤,
공명이 되고 탄소음이온이 양성자를 냠냠한다
<3> H H (catalytic hydrogenation)
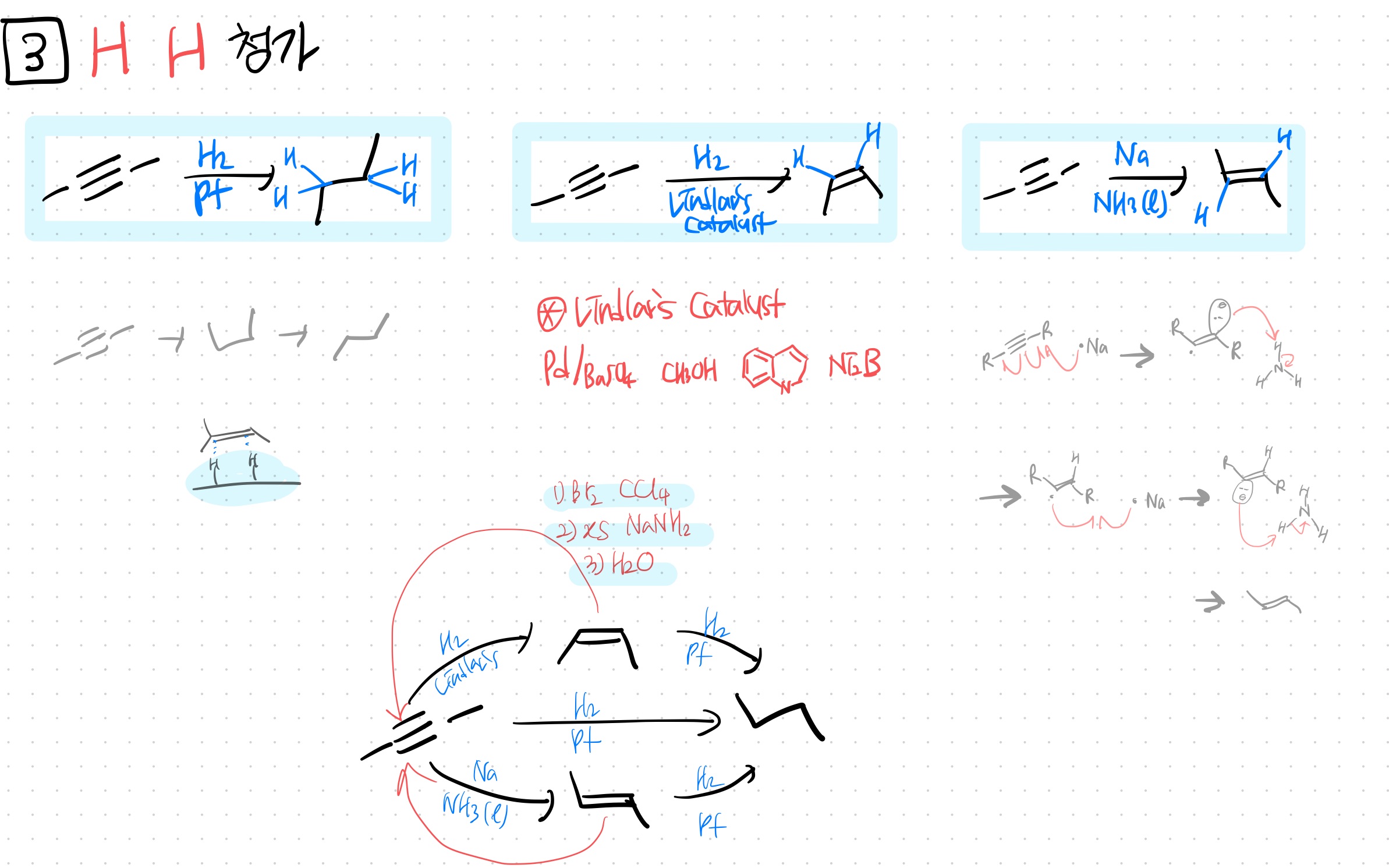
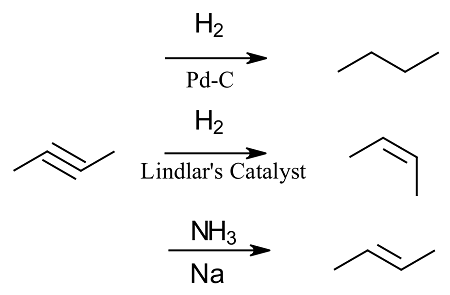
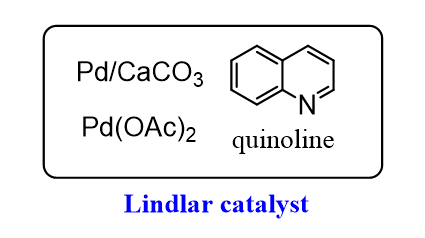
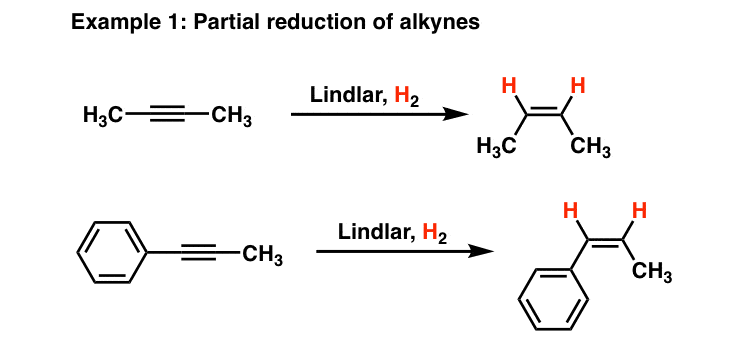
(1) H2, Lindlar's catalyst
cis한 alkene
alkane까지 가기 싫고 alkene에서 멈추고 싶을 때.
특히 cis한 alkene을 만들고 싶을 때 Lindlar's catalyst를 이용한다
(3) Na NH3
trans한 alkene
alkane까지 가기 싫고 alkene에서 멈추고 싶을 때.
특히 trans한 alkene을 만들고 싶을 떄
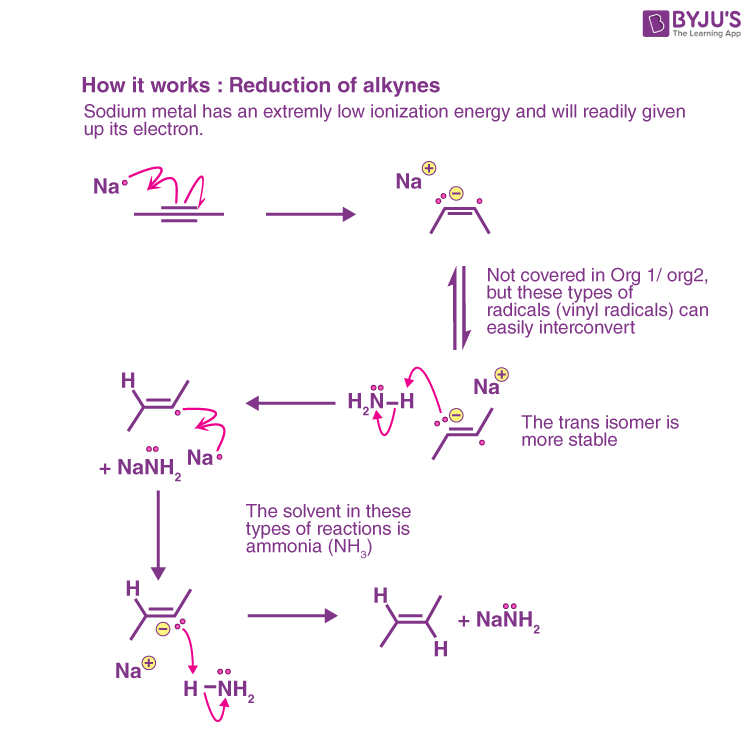
라디칼을 거치기 때문에 trans해진다. radical과 고립전자쌍이 엇갈린게 좋아서 그렇다
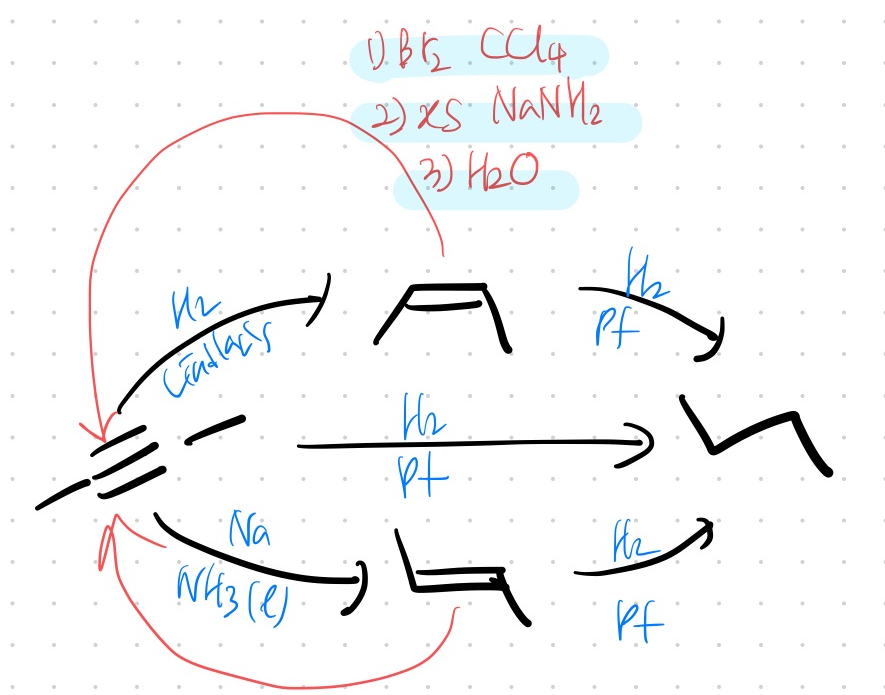
요약하자면 이런 관계다.
한 편 alkene에서 alkyne을 만들 수도 있는데,
alkene을 X2 첨가반응 해서 dihalide를 만든 후
앞서 봤던 alkyne 생성반응을 이용하면 된다!
<4> X X
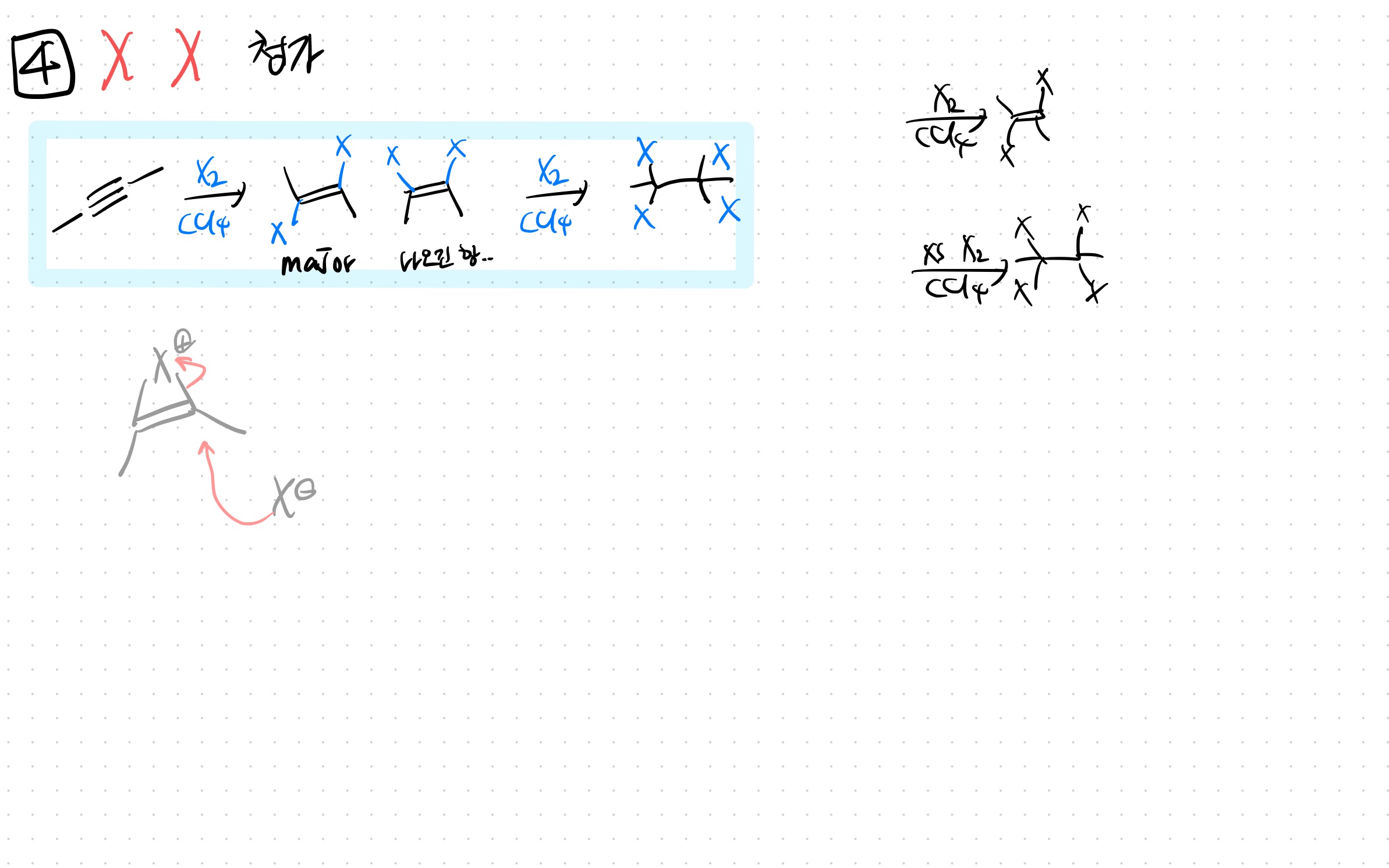
X2 (halogenation)
-1당량이면 alkene **trans alkene이 major
-2당량(혹은 xs)이면 alkane
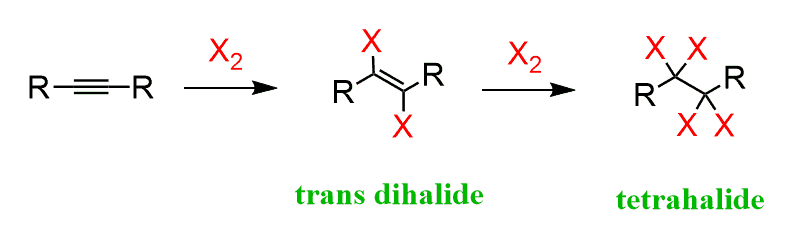
trans alkene이 major다.
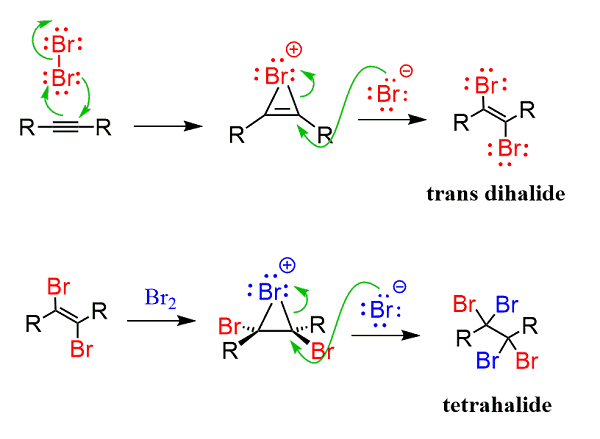
alkene처럼 X가 양쪽과 결합을 이루기 때문에, 이후 SN2 반응을 하며 trans한 alkene이 더 major가 된다
특이한 점은 cis alkene도 minor지만 나오긴 한다
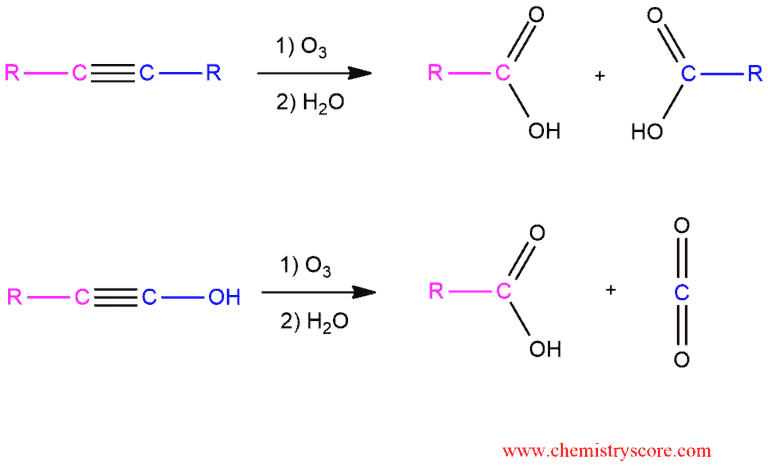
<6> Ozonolysis
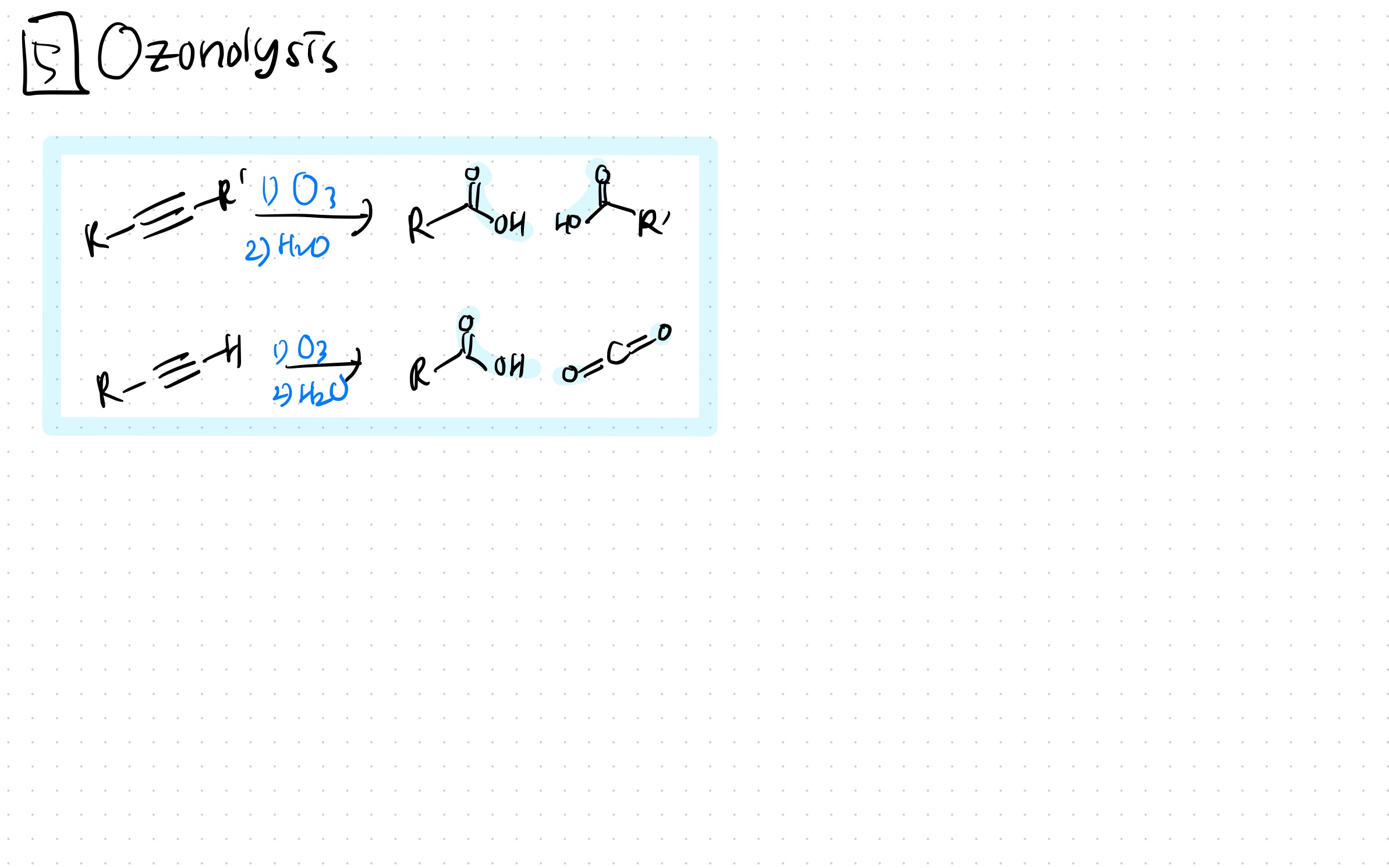
첨가 반응 외에도 Ozonolysis가 있음
1) O3
2) H2O
이중결합 자리가..
-R기일 땐 카복실산
-H일 땐 CO2가 된다
'유기화학' 카테고리의 다른 글
| 유기화학 강의 11. 합성 연습 문제 (0) | 2025.01.04 |
|---|---|
| [유기 화학] 9. Radical 반응 (0) | 2024.07.31 |
| [유기 화학] 7. Alkene 첨가 반응 (0) | 2024.07.25 |
| [유기 화학] 6. Alkyl halide의 치환/제거 반응: SN2 SN1 E2 E1 (7) | 2024.07.24 |
| [유기 화학] 5. 합성 반응에 필요한 기본 개념 (6) | 2024.07.24 |



댓글