영상강의
Alkene의 명명법과 성질
<Alkene의 명명법>
Alkane과 다른 점 몇 가지만 알면 된다.
1. 모체는 2중결합이 있는 것 中 가장 긴 것이어야 한다.
2중 없는 것 중 더 긴게 있더라도.. 걘 모체가 될 수 없음
-ene으로 끝내고, 2중결합의 번호를 함께 써준다
ex. 2-heptene 혹은 hept-2-ene
2. E/Z를 쓸 수 있다면 쓴다
양쪽의 작용기에서, 우선순위가 큰(원자번호가 큰) 작용기끼리 같은 방향이면 Z, 다른 방향이면 E이다.
(E)- 이런식으로 나타내면 됨
R,S도 나타내야 한다면, R/S를 E보다 먼저 쓴다
ex. (R)-(E)- ~~~
사진 속 예제는 예를 들어서
1. 2중 결합 있는 것 중 가장 긴 건 7개 >> heptene
2. 첫 작용기 숫자 최소가 되도록 번호 매김 >>hept-3-ene
3. 작용기들 이름 매기고, 알파벳 순으로 나열 >> 1-chloro-2,3-dimethylhept-3-ene
4. E/Z 나타내줌 >> (E)-1-chloro-2,4-dimethylhept-3-ene
<Alkene의 안정성>
* substituted가 많이 될수록
* Steric한 작용기끼리 어긋난 구조일수록
Alkene 첨가 반응
Alkene의 2중결합은 전자가 많기 때문에, 친핵체나 염기로 작용한다.
따라서 2중결합 대신 작용기 2개가 붙으며 첨가 반응이 일어날 수 있다.
| H, X | H OH | H H | X X | X OH | OH OH |
| Markovnikov rearrangement racemic HX |
Markovnikov rearrangement [H2SO4] 등 산성 |
syn H2, Pt 혹은 Willkinson's Catalyst |
anti X2 |
Markovnikov anti X2, H2O(용매) |
syn 1) RCO3H 2) H2SO4 (산성) |
| anti-Markovnikov racemic HBr ROOR |
Markovnikov rearrangement X 1) Hg(OAC)2, H2O 2) NaBH4 |
anti OsO4, Na2SO3/NaHSO3/NMO 혹은 KMnO4, base (cold) |
|||
| anti-Markovnikov syn 1) BH3 THF 2)H2O2 NaOH |
<1> H X (hydrohalogenation)
HX와 반응
-Markovnikov : 치환기 많은 쪽에 X, 적은 쪽에 H
-rearrangement : 탄소양이온을 거치기 때문
-racemic : 탄소양이온을 거치기 때문


HBr의 H와 먼저 반응하고 탄소 양이온을 거치게 되는데,
탄소 양이온은 차수가 높을수록 좋아해서 차수 높은 쪽에 생김.
거기를 친핵체인 Br-가 공격해 차수가 높은 쪽이 Br이 됨.
탄소양이온일 때 Br-가 공격해서, 양쪽면에 접근이 가능하기 때문에 결과물이 racemic함.
탄소양이온을 거치기 때문에 rearrangement가 가능함
-rearrangement는 저번에 배웠듯: (1)더 높은 차수나 allyl/benzyl이 될 때 (2)더 큰 고리가 될 수 있을 때

HX, ROOR과 반응
-anti Markovnikov : 치환기 많은 쪽에 H, 적은 쪽에 X (radical을 거치기 때문)
-racemic


메커니즘을 보면, OR에 의해 라디칼이 된 Br이 H보다 먼저 반응한다.
그로 인해 생기는 (구)알켄의 라디칼.. 라디칼도 3차>2차>1차일수록 안정하기 때문에(hyperconjugation) 나중에 붙는 H가 차수가 높은 곳에 붙게 된다.
<2> H OH (hydration)
(1) H2SO4 등.. (Acid-Catalyzed)
-Markovnikov : 치환기 많은 쪽에 OH, 적은 쪽에 H
-rearrangement : 탄소양이온을 거치기 때문
-racemic : 탄소양이온을 거치기 때문
**산성 조건 하, H2O 대신 다른 H-Nuc과 반응하면 H Nuc으로 첨가 됨

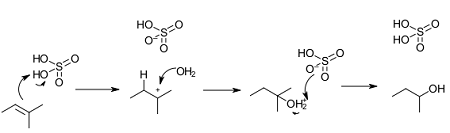
H3O+의 H+와 먼저 반응해 탄소양이온을 생성.
역시 차수가 높은 쪽이 탄소양이온이 됨
그 뒤 H2O가 친핵체로 작용해 탄소양이온 자리에 붙음. 따라서 차수가 높은 쪽에 OH가 붙게 됨.
마찬가지로 탄소양이온을 거쳐서 rearrangement, racemic함
***속도

알켄치환반응과 E2반응이 서로 정반응-역반응 관계임
어떤 조건이냐에 따라, 평형의 위치가 달라짐
diluted한 산성 용액 (H2O 적음), 저온 - 알켄치환반응 유리
conc한 산성 용액(H2O 많음), 고온 - E2반응 유리
H2O가 많고 적고에 따라, 르샤틀리에의 원리에 의해 유리한 반응이 달라짐
치환반응 기준 계의 엔트로피 감소(분자수 감소), 계의 엔탈피 감소=발열반응(파이결합이 더 강한 시그마 결합으로 변함)
따라서 저온일수록 치환반응이 유리함
(2) 1) Hg(OAc)2 H2O
2) NaBH4
(oxymercuration demercuration)
-Markovnikov : 치환기 많은 쪽에 OH, 적은 쪽에 H
-rearrangement XXXXXXXXXXXX
*** H2O 대신 다른 H-Nuc과 반응하면 H Nuc으로 첨가 됨


메커니즘을 보면, Hg가 파이결합의 양쪽과 결합을 이룬다(그러나 치환이 덜 된 쪽과 더 세게 결합한다)
그래서 탄소양이온이 완전하지 못하고 partial하게 된다 -> rearrangement를 하기에 양전하가 부족하다
따라서 rearrangement가 일어나지 않게 된다.
(3) 1) BH3 THF
2) H2O2 NaOH
(hydroboration oxidation)
-anti-Markovnikov : 치환기 적은 쪽에 OH, 많은 쪽에 H : BH3가 2중결합 양쪽에 동시에 접근하게 되는데, steric하지 않은 치환기가 적은 쪽에 - BH2가 붙고, 그게 OH로 바뀌게 된다
-syn : BH3의 H와 BH2가 동시에 접근해서 syn하게 된다.
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)

이 경우엔 양쪽 이중결합 모두 chiral C가 되어, chiral C가 2개가 생긴다.
따라서 입체 이성질체를 4개 가질 수 있는데, 그 중 2개의 입체이성질체가 나오게 된다.

이처럼 BH2는 steric해서 덜 치환된 곳에, H는 치환이 많이 된 곳에 붙게 된다
(또 BH2가 미세하게 먼저 붙어서 덜 치환된 곳에 붙음. 치환 많이 된 곳에 탄소 양이온 생기라고)
그래서 anti-Markovnikov가 됨
그리고 동시에 붙으니까, syn하게 붙음.
즉 같은 평면 쪽으로 붙게 됨.
racemic하지 못하다!
<3> H H (catalytic hydrogenation)
H2, Pt
혹은 Willkinson's Catalyst
(catalytic hydrogenation)
-H, H로 똑같은 애들이 붙어서 Markovnikov 생각 안해도 됨
-syn
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)
단, mesocompound라면 3개 中 1개

이처럼 syn하게 붙음. 이 경우엔 2개의 chiral C가 생기게 되는데, 대칭면이 있어서 meso compound임.
그래서 위로 붙으나 아래로 붙으나 똑같음. 따라서 3개의 입체 이성질체 중 1개의 입체 이성질체가 생기는 셈
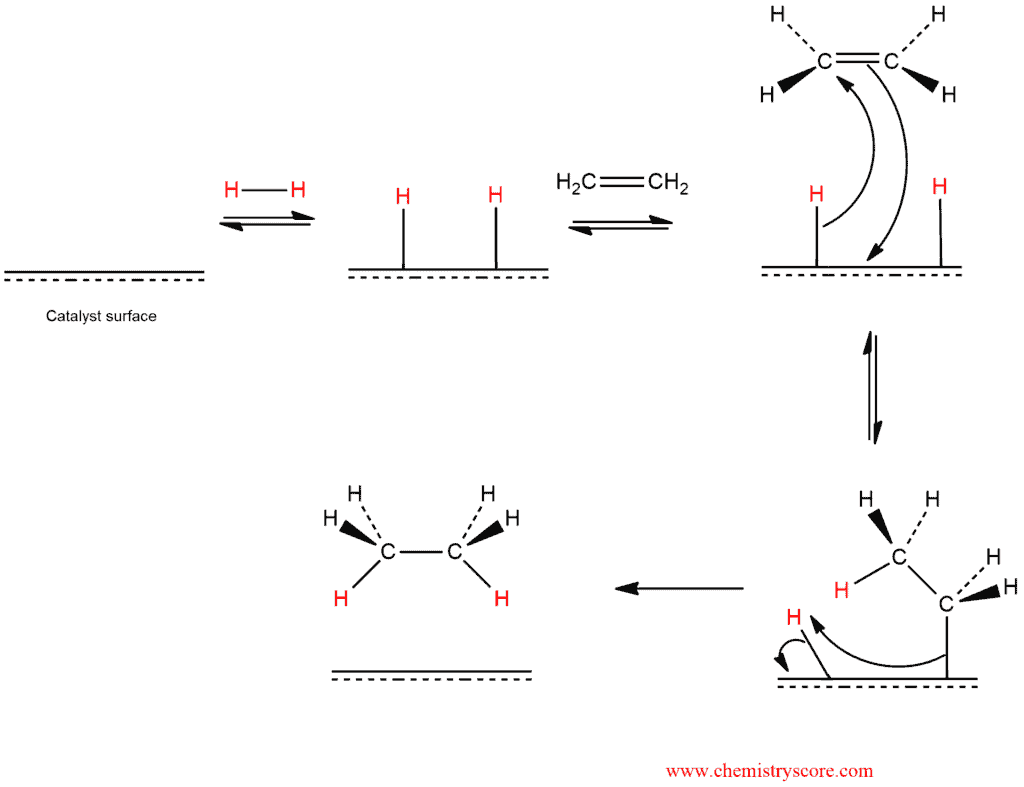
이처럼 금속 촉매에 달린 H가 같은 평면 상 붙기 때문에 syn하다

willkinson's catalyst는 이런 식으로 생김
만약 enantiomer 중 하나에 해당하는 비대칭한 willkinson's catalyst를 쓰게 되면, syn한 2가지 결과물 중 하나가 더 우세하게 나타나기도 함
<4> X X 혹은 X OH
(1) X2 (halogenation)
-X, X로 똑같은 애들이 붙어서 Markovnikov 생각 안해도 됨
-anti
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)
단, mesocompound라면 3개 中 1개

이처럼 X2는 anti하게 붙음.
이 경우엔 chiral C 2개, meso인 경우라 3개 중 1개의 입체이성질체가 나타난 셈

이렇게 Br+가 양쪽과 동시에 붙어 있고, 그 중 하나를 Br-가 친핵성 공격하면서 떨어져서 SN2처럼 반응하게 됨
따라서 둘이 정반대의 방향인 anti한 방식으로 붙는 거임
(2) X2, H2O (halohydrin)
-Markovnikov : 치환 많이 된 쪽에 OH
-anti
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)
*** H2O 대신 다른 H-Nuc과 반응하면 X Nuc으로 첨가 됨

이처럼 Markovnikov하게, 치환 많이 된 쪽에 OH가 붙음
또, anti로 붙음

메커니즘 초반은 X2와 같음. Br+가 이중결합 양쪽에 팔을 가지고 있음. 단, 치환 덜 된 쪽과 더 강한 결합을 하고 있을 것.
그런데 이 경우에는 Br-가 공격하기 전에, 용매라 잔뜩 있는 H2O가 친핵성 공격을 하게 됨
이 경우에도 SN2처럼 반응해서 backside attack을 하기 때문에 anti한 방식으로 붙게 됨
<5> OH OH (dihydroxylation)
(1) 1)RCO3H
2)H2SO4 등 산
-OH, OH로 똑같은 애들이 붙어서 Markovnikov 생각 안해도 됨
-anti
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)
단, mesocompound라면 3개 中 1개

이처럼 trans하게 붙음
이 경우는 meso하지 않아서 4 중 2

X2 경우와 유사하게, O가 양쪽과 결합하고 있고, 그 뒤 SN2하게 H2O가 반응해서 anti하게 붙음
(2) KMnO4, basic (cold)
혹은 1)OsO4 2)Na2SO3/NaHSO3/NMO
-OH, OH로 똑같은 애들이 붙어서 Markovnikov 생각 안해도 됨
-syn
*** 그 결과 chiral C가
0개면 : 입체 고려할 필요X
1개면 : 2개의 enantiomer 중 2개의 enantiomer
2개면 : 4개의 입체이성질체 중 2개의 입체이성질체 (1쌍의 enantomer)
단, mesocompound라면 3개 中 1개

이처럼 syn하게 붙는다

BH3 때처럼 동시에 붙어서 syn하게 붙음
**막간 tip!
syn하게 붙는 애들은 cis한 애랑 반응할 때 meso
anti하게 붙는 애들은 trans한 애랑 반응할 때 meso
<6> Ozonolysis
첨가 반응 외에도 Ozonolysis가 있음
1) O3
2) DMS 혹은 Zn/H3O+
이중결합 자리가.. 둘 다 O와 이중결합을 이룬 것으로 바뀜

'유기화학' 카테고리의 다른 글
| [유기 화학] 9. Radical 반응 (0) | 2024.07.31 |
|---|---|
| [유기 화학] 8. Alkyne 첨가 반응 (0) | 2024.07.29 |
| [유기 화학] 6. Alkyl halide의 치환/제거 반응: SN2 SN1 E2 E1 (7) | 2024.07.24 |
| [유기 화학] 5. 합성 반응에 필요한 기본 개념 (6) | 2024.07.24 |
| [유기 화학] 4. 입체화학, 이성질체 - 구조이성질체, 입체이성질체(거울쌍이성질체, 부분입체이성질체) (2) | 2024.07.18 |




댓글