줌달의 일반화학 정리 10판 솔루션
<화학의 초기 역사>
*3가지 법칙
Lavoisier의 질량 보존의 법칙 : 물질은 창조, 소멸되지 않음
Proust의 일정 성분비의 법칙 : 주어진 화합물 내 원소들의 질량비는 일정함 (화합물의 일정한 조성)
Dalton의 배수 비례의 법칙 : 두 원소로 이루어진 다양한 화합물에서..
한 원소 A 1g에 대한 다른 원소 B의 질량은 간단한 정수비 >> 원자의 상대질량표

*Dalton의 원자론
1. 각 원소는 원자로 이루어짐
2. 같은 원소의 원자는 같다, 다른 원소의 원자는 다르다
3. 화합물은 원자 간 결합으로 형성되고, 화합물은 일정한 조성을 가진다
4. 화학 반응은 원자들의 재편성으로, 결합이 변하지 원자 자체는 변하지 않는다
<원자에 대한 초기 실험>
*Thomson - 음극선관 실험 - 전자

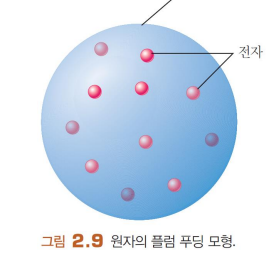
다양한 금속에서 전극이 유래 - 모든 원자는 전자를 가진다
음극선이고, 음극과 반발하며 양극으로 휜다 - 음전하
휘는 정도 - 전하/질량 비 계산함
모든 원자는 전기적 중성 - 원자는 양전하를 가진다 >> 플럼푸딩모형
*Millikan - 기름대전 실험 - 전하량, 질량

X선 가해 대전.. 최대공약수가 전자의 전하량일 것이다
*Rutherford - 알파입자산란실험 - 원자핵
Becquerel의 방사능을 바탕으로 함 - 알파 입자는 질량이 크고 양전하를 가짐
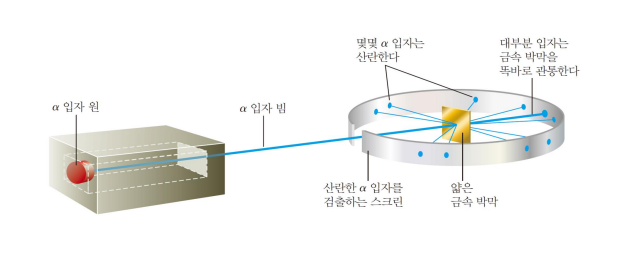

몇 알파입자가 굴절 혹은 반사 - 밀도가 크고 크기가 작은 양전하의 무언가가 원자 중앙에 있다
*현재적 관점


매우 작은 중앙의 핵(양성자+중성자)과 핵 주위를 돌아다니는 전자
전자가 화학적 성질(다른 원자와 상호작용 하는 능력)을 결정
질량수 : 양성자+중성자 개수
원자 번호 : 양성자 개수
동위원소 : 양성자 수(원자번호) 같지만 중성자 수(질량수 영향)는 다름
<분자와 이온>
원자 간 결합방식에 따른 화합물 차이
| 분자 (공유결합) | 이온 (이온결합) |
| 전자를 공유 H2, H2O, NH3.. -구조식 -공간채움모형 -공막대모형 ... |
대전된 양이온, 음이온 간 인력 NaCl, NH4NO3 -이온성 고체(염) ... |
<주기율표>


금속: 열, 전기전도성, 연성, 전성, 광택...
준금속
비금속
1A 알칼리 금속 - 리튬(Li), 소듐(Na), 포타슘(K), 루비듐(Rb), 세슘(Cs), 랑슘(Fr)
2A 알칼리 토금속 - 베릴륨(Be), 마그네슘(Mg), 칼슘(Ca), 스트론튬(Sr), 바륨(Ba), 라듐(Ra)
7A 할로젠 원소 - 플루오린(F), 염소(Cl), 브로민(Br), 아이오딘(I), 아스타틴(At)
8A 불활성 기체 - 헬륨(He), 네온(Ne), 아르곤(Ar), 크립톤(Kr), 제논(Xe), 라돈(Rn)
<화합물의 명명법>
아래 링크에 따로 정리
'일반화학 > 일반화학 개념정리' 카테고리의 다른 글
| <일반 화학> 6장- 열역학 (0) | 2023.05.09 |
|---|---|
| <일반 화학> 5장- 기체 (0) | 2023.05.08 |
| <일반 화학> 4장- 화학반응의 종류와 용액의 화학량 (0) | 2023.05.08 |
| <일반 화학> 3장- 화학량론 (1) | 2023.05.08 |
| <일반 화학> 1장 - 화학의 기초 (1) | 2023.05.01 |




댓글